Atomski radijus kako se mjeri, kako se mijenja u periodnom sustavu, primjeri
atomski polumjer to je važan parametar za periodična svojstva elemenata periodnog sustava. To je izravno povezano s veličinom atoma, budući da su na većem radijusu veći ili glomazniji. Isto tako, ona je povezana s elektroničkim karakteristikama istih.
Sve dok atom ima više elektrona, veća je njegova veličina i atomski polumjer. Oba su definirana elektronima valentne ljuske, jer na udaljenosti izvan njihovih orbita vjerojatnost pronalaženja elektrona približava se nuli. U blizini jezgre javlja se suprotno: povećava se vjerojatnost pronalaženja elektrona.

Gornja slika predstavlja pakiranje pamučnih kuglica. Imajte na umu da je svaki okružen sa šest susjeda, ne računajući drugi mogući gornji ili donji red. Način na koji se vrećice pamuka zbijaju definirat će njihove veličine, a time i njihove radijuse; kao što se događa s atomima.
Elementi prema njihovoj kemijskoj prirodi na jedan ili drugi način međusobno djeluju s vlastitim atomima. Stoga se veličina atomskog radijusa mijenja ovisno o vrsti prisutne veze i čvrstom pakiranju njegovih atoma.
indeks
- 1 Kako se mjeri atomski radijus?
- 1.1. Određivanje internuklearne udaljenosti
- 1.2 Jedinice
- 2 Kako se mijenja periodni sustav?
- 2.1 Tijekom razdoblja
- 2.2 Spuštanje grupe
- 2.3 Kontrakcija lantanida
- 3 Primjeri
- 4 Reference
Kako se mjeri atomski radijus?
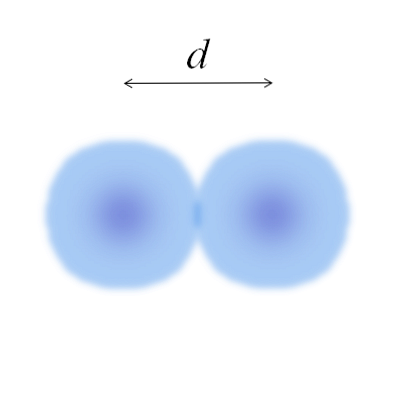
Na glavnoj slici može se lako izmjeriti promjer vate, a zatim ga podijeliti na dva. Međutim, sfera atoma nije u potpunosti definirana. Zašto? Budući da elektroni cirkuliraju i difundiraju u specifičnim područjima prostora: orbitale.
Dakle, atom se može smatrati kuglom s neopipivim rubovima, što je nemoguće sa sigurnošću reći u kojoj mjeri završavaju. Na primjer, u gornjoj slici središnja regija, u blizini jezgre, izgleda intenzivnije boje, dok su joj rubovi zamagljeni..
Slika predstavlja dvoatomsku molekulu E2 (kao Cl2, H2, O2, itd.) Pod pretpostavkom da su atomi sferična tijela, ako je udaljenost određena d koja razdvaja obje jezgre u kovalentnoj vezi, onda bi bilo dovoljno da se podijeli na dvije polovice (d/ 2) za dobivanje atomskog radijusa; točnije, kovalentni radijus E za E2.
A ako E ne formira kovalentne veze sa samim sobom, već je to metalni element? tada d na to bi ukazivao broj susjeda koji okružuju E u svojoj metalnoj strukturi; to jest, koordinacijskim brojem (N.C) atoma unutar pakiranja (zapamtite pamučne kuglice glavne slike).
Određivanje internuklearne udaljenosti
Da odredimo d, što je među-jezična udaljenost za dva atoma u molekuli ili pakiranju, to zahtijeva tehnike fizičke analize.
Jedna od najčešće korištenih je difrakcija X-zraka, u kojoj se zrakom zrači zrak snopa kroz kristal i proučava se difrakcijski uzorak koji je rezultat interakcije između elektrona i elektromagnetskog zračenja. Ovisno o pakiranju, mogu se dobiti različiti difrakcijski uzorci i, prema tome, druge vrijednosti d.
Ako su atomi "čvrsto" u kristalnoj rešetki, oni će predstavljati različite vrijednosti d u usporedbi s onim što bi imali da su "udobni". Također, ove internuklearne udaljenosti mogu oscilirati u vrijednostima, tako da se atomski radijus zapravo sastoji od prosječne vrijednosti takvih mjerenja.
Kako su povezani atomski radijus i koordinacijski broj? V. Goldschmidt je uspostavio odnos između ta dva, u kojima je za N.C. od 12 relativna vrijednost 1; od 0,97 za pakiranje gdje atom ima N.C jednako 8; 0,96, za NC jednako 6; i 0,88 za NC od 4.
jedinice
Iz vrijednosti za N.C jednako 12, konstruirane su mnoge tablice u kojima se uspoređuju atomski radijusi svih elemenata periodnog sustava..
Kako svi elementi ne tvore takve kompaktne strukture (NC manje od 12), odnos V. Goldschmidta koristi se za izračunavanje njihovih atomskih radijusa i njihovo izražavanje za isto pakiranje. Na taj način, mjerenja atomskih radijusa su standardizirana.
Ali u kojim se jedinicama izražavaju? s obzirom da d je vrlo male veličine, treba upotrijebiti jedinice angstroma Å (10. 10-10m) ili također široko korišten, pikometar (10. 10-12m).
Kako se mijenja periodni sustav?
Tijekom razdoblja
Atomski radijusi određeni za metalne elemente dobivaju ime metalnog radijusa, dok za one nemetalne elemente kovalentni radijusi (kao što je fosfor, P)4, ili sumpor, S8). Međutim, između oba tipa radija postoji izraženija razlika od naziva.
S lijeva na desno u istom razdoblju, jezgra dodaje protone i elektrone, ali potonji su ograničeni na istu razinu energije (glavni kvantni broj). Kao posljedica toga, nukleus izaziva povećanje efektivnog nuklearnog naboja na valentne elektrone, koji kontrahiraju atomski radijus.
Na taj način nemetalni elementi u istom razdoblju imaju tendenciju da imaju atomske (kovalentne) radijuse manje od metala (metalni radijusi).
Spuštanje grupe
Kada se spušta skupina, omogućuju se nove razine energije, koje omogućuju elektronima da imaju više prostora. Dakle, elektronički oblak pokriva veće udaljenosti, a njegova zamagljena periferija završava sa udaljavanjem više od jezgre, te se stoga atomski polumjer širi..
Kontrakcija lantanida
Elektroni unutarnjeg sloja pomažu zaštititi učinkovito nuklearno punjenje na valentnim elektronima. Kada orbitale koje sačinjavaju unutarnje slojeve imaju mnogo "rupa" (čvorova), kao i kod f orbitala, jezgra snažno kontrahira atomski polumjer zbog lošeg zaštitnog učinka orbitala..
Ta činjenica je dokazana u kontrakciji lantanida u razdoblju 6 periodnog sustava. Od La do Hf postoji znatna kontrakcija atomskog radijusa proizvedenog orbitalima f, koji "popunjavaju" kako prolazi kroz blok f: onaj lanthanoida i aktinoida.
Sličan učinak može se promatrati i sa elementima bloka p iz perioda 4. Ovaj vremenski proizvod slabog zaštitnog učinka orbitala d koji se pune pri križanju razdoblja prijelaznih metala.
Primjeri
Za razdoblje 2 periodnog sustava atomski radijusi njegovih elemenata su:
-Li: 257 sati
-Budite: 112 sati
-B: 88 pm
-C: 77 pm
-N: 74 pm
-O: 66 pm
-F: 64 p.m.
Treba napomenuti da litijev metal ima najveći atomski radijus (257 p.m.), dok je fluor, koji se nalazi na krajnjem desnom dijelu razdoblja, najmanji od njih (64 sata). Atomski polumjer se spušta s lijeva na desno u istom razdoblju, a navedene vrijednosti pokazuju.
Litij, formiranjem metalnih veza, njegov je radijus metalik; i fluor, budući da tvori kovalentne veze (F-F), njegov radijus je kovalentan.
A ako želite izraziti atomski radio u jedinicama angstroma? Jednostavno ih podijelite na 100: (257/100) = 2.57Å. I tako dalje s ostalim vrijednostima.
reference
- Kemija 301. Atomska radija. Preuzeto s: ch301.cm.utexas.edu
- Temelj CK-12. (28. lipnja 2016.) Atomski radijus. Preuzeto s: chem.libretexts.org
- Trendovi u atomskim radijima. Preuzeto s: intro.chem.okstate.edu
- Clackamas Community College. (2002). Atomska veličina. Preuzeto s: dl.clackamas.edu
- Clark J. (kolovoz 2012). Atomski i ionski polumjer. Preuzeto s: chemguide.co.uk
- Shiver & Atkins. (2008). Anorganska kemija (Četvrto izdanje, str. 23, 24, 80, 169). Mc Graw Hill.


