Svojstva, struktura, uporaba i rizici kalijevog jodoata
kalijev jodat ili kalijev jodat je anorganski spoj joda, posebno sol, čija je kemijska formula KIO3. Jod, element skupine halogena (F, Cl, Br, I, As), ima u ovoj soli oksidacijski broj od +5; zbog toga je jako oksidacijsko sredstvo. KIO3 disocira u vodenom mediju kako bi se stvorili K ioni+ i IO3-.
Sintetizira se reakcijom kalijevog hidroksida s jodnom kiselinom: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Također se može sintetizirati reakcijom molekulskog joda s kalijevim hidroksidom: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

indeks
- 1 Fizikalna i kemijska svojstva
- 1.1 Oksidirajuće sredstvo
- 2 Kemijska struktura
- 3 Uporaba i primjena kalijevog jodata
- 3.1 Terapeutska uporaba
- 3.2 Uporaba u industriji
- 3.3. Analitička uporaba
- 3.4 Korištenje u tehnologiji lasera
- 4 Opasnost po zdravlje od kalijevog jodata
- 5 Reference
Fizikalna i kemijska svojstva
Bijela čvrsta tvar bez mirisa, s finim kristalima i kristalnom strukturom monoklinskog tipa. Ima gustoću od 3,98 g / ml, molekularnu težinu od 214 g / mol i apsorpcijske vrpce u infracrvenom (IR) spektru..
Ima talište: 833 ºK (560 ºC), u skladu s jakim ionskim interakcijama između iona K+ i IO3-. Pri višim temperaturama prolazi toplinsku reakciju razgradnje, oslobađajući molekulski kisik i kalijev jodid:
2KIO3(s) => 2KI (s) + 3O2(G)
U vodi ima topljivost koja varira od 4,74 g / 100 ml do 0 ºC, do 32,3 g / 100 ml na 100 ºC, stvarajući bezbojne vodene otopine. Osim toga, netopljiv je u alkoholu i dušičnoj kiselini, ali je topljiv u razrijeđenoj sumpornoj kiselini.
Njegov afinitet prema vodi nije značajan, što objašnjava zašto nije higroskopan i ne postoji u obliku hidratiranih soli (KIO)3· H2O).
Oksidirajuće sredstvo
Kalijev jodat, kao što pokazuje njegova kemijska formula, ima tri atoma kisika. To je jako elektronegativni element i zbog tog svojstva "otkriva" elektronički nedostatak u oblaku koji okružuje jod.
Ovaj nedostatak - ili doprinos, ovisno o slučaju, može se izračunati kao oksidacijski broj joda (± 1, +2, +3, +5, +7), što je +5 za slučaj te soli..
Što to znači? Da će jod prije vrste koja može dati svoje elektrone prihvatiti ih u svom ionskom obliku (IO)3-) postati molekularni jod i imati oksidacijski broj jednak 0.
Nakon ovog objašnjenja može se utvrditi da je kalijev jodat oksidirajući spoj koji snažno reagira s redukcijskim sredstvima u mnogim redoks reakcijama; od svih ovih, jedan je poznat kao jodni sat.
Sat s jodom sastoji se od redoks procesa sporog i brzog koraka, pri čemu su brzi koraci označeni KIO rješenjem3 u sumpornoj kiselini kojoj se dodaje škrob. Zatim, škrob - jednom proizveden i usidren između njegove strukture I vrste3-- pretvorit će otopinu iz bezbojne u tamno plavu.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6H+ → 3 I2 + 3H2O
ja2 + tna3- + H2O → 2 I- + tna4- + 2H+ (tamno plava zbog učinka škroba)
Kemijska struktura
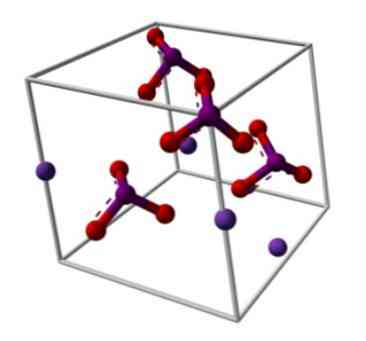
Kemijska struktura kalijevog jodata prikazana je na gornjoj slici. 10 anion3- predstavlja "tronožac" crvenih i ljubičastih sfera, dok su ioni K+ oni su predstavljeni ljubičastim sferama.
Ali što znače ti stativi? Pravi geometrijski oblici tih aniona zapravo su trigonalne piramide, u kojima kisici čine trokutnu bazu, a ne-zajednički par elektrona u jodu pokazuje prema gore, zauzimajući prostor i prisiljavajući IO vezu dolje i dva veze I = O.
Ova molekularna geometrija odgovara sp hibridizaciji3 središnjeg jodnog atoma; međutim, druga perspektiva sugerira da jedan od atoma kisika formira veze s "d" orbitalima joda, budući da je u stvari sp hibridizacija3d2 (jod može imati svoje "d" orbitale koje šire svoju valentnu ljusku).
Kristali ove soli mogu se podvrgnuti prijelazima strukturne faze (drugim rasporedima od monoklinske) kao posljedica različitih fizičkih uvjeta koji ih podvrgavaju.
Uporaba i primjena kalijevog jodata
Terapijska uporaba
Kalijev jodat se obično koristi za sprječavanje nakupljanja radioaktivnosti u štitnjači u obliku 131I, kada se taj izotop koristi za određivanje unosa joda od strane štitne žlijezde kao komponente funkcioniranja štitne žlijezde.
Isto tako, kalijev jodat se koristi kao topikalni antiseptik (0,5%) u infekcijama sluznice..
Koristi se u industriji
Dodaje se hrani domaćih životinja kao dodatak jodu. Stoga se u industriji koristi kalijev jodat za poboljšanje kvalitete brašna.
Analitička uporaba
U analitičkoj kemiji, zahvaljujući svojoj stabilnosti, koristi se kao primarni standard u standardizaciji standardnih otopina natrijevog tiosulfata (Na2S2O3), kako bi se odredile koncentracije joda u uzorcima.
To znači da količine joda mogu biti poznate putem volumetrijskih tehnika (titracija). U ovoj reakciji kalijev jodat brzo oksidira jodidne ione-, sljedećom kemijskom jednadžbom:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jod, ja2, naslovljen s otopinom Na2S2O3 za njegovu standardizaciju.
Koristi se u tehnologiji lasera
Istraživanja su pokazala i potvrdila zanimljiva piezoelektrična, piroelektrična, elektrooptička, feroelektrična svojstva iu nelinearnoj optici KIO kristala3. To rezultira velikim potencijalom u elektroničkom polju i tehnologiji lasera za materijale izrađene s ovim spojem.
Zdravstveni rizici kalijevog jodata
U visokim dozama može uzrokovati iritaciju sluznice usne šupljine, kože, očiju i dišnih putova.
Pokusi toksičnosti kalijevog jodata kod životinja dopustili su uočiti da kod pasa na postu, u dozama od 0,2 do 0,25 g / kg tjelesne težine, koje se daju oralno, spoj uzrokuje povraćanje.
Ako se izbjegaju ove povraćanje, to uzrokuje pogoršanje situacije u životinja, jer izaziva anoreksiju i prostoriju prije smrti. Njegove autopsije dopuštale su promatranje nekrotičnih lezija u jetri, bubrezima i crijevnoj sluznici.
Zbog svoje oksidacijske snage predstavlja opasnost od požara kada dođe u kontakt sa zapaljivim materijalima.
reference
- Day, R., & Underwood, A. Kvantitativna analitička kemija (peti red.). PEARSON Prentice Hall, str.
- Muth, D. (2008). Laseri. Preuzeto s: flickr.com
- ChemicalBook. (2017). Kalijev jodat. Preuzeto 25. ožujka 2018. iz tvrtke ChemicalBook: chemicalbook.com
- Pubchem. (2018.). Kalijev jodat. Preuzeto 25. ožujka 2018. iz PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018.). Kalijev jodat. Preuzeto 25. ožujka 2018. godine iz tvrtke Merck:
- merckmillipore.com
- Wikipedia. (2017). Kalijev jodat. Preuzeto 25. ožujka 2018. s Wikipedije: en.wikipedia.org
- M. Abdel Kader i sur. (2013). Mehanizam prijenosa naboja i niskotemperaturni fazni prijelazi u KIO3. J. Phys., Conf. Ser 423 012036


