Svojstva natrijevog hidrida (NaH), reaktivnost, opasnosti i uporabe
natrijev hidrid R3 je anorganski spoj formule NaH. Ima ionsku vezu između natrija i hidrida. Njegova struktura prikazana je na slici 1. Ona je reprezentativna za slane hidride, što znači da je hidrid sličan soli, sastavljen od Na + i H-iona, za razliku od molekularnih hidrida kao što su boran, metan, amonijak i vode.
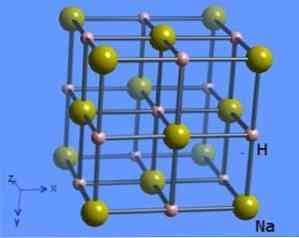
Kristalna struktura ima koordinacijski broj 6, gdje je svaka natrijeva molekula okružena sa 8 hidridnih iona koji imaju oktaedarski oblik i prikazana je na slici 2 (Mark Winter [Sveučilište u Sheffieldu i WebElements Ltd, 1993-2016).
Spoj se pripravlja izravnom reakcijom između natrija i plina vodika (natrijeva hidridna formula - upotreba, svojstva, struktura i formula natrijevog hidrida, 2005-2017) kako slijedi:
H2 + 2Na → 2NaH
Natrijev hidrid se komercijalno prodaje kao oblik disperzije 60% w / w (postotak težine) u mineralnom ulju za sigurno rukovanje (SODIUM HYDRIDE, s.f.).
indeks
- 1 Fizikalna i kemijska svojstva natrijevog hidrida
- 2 Reaktivnost i opasnosti
- 3 Upotreba
- 4 Reference
Fizikalna i kemijska svojstva natrijevog hidrida
Natrijev hidrid je bijela krutina kada je čista, iako se općenito dobiva u sivoj ili srebrnoj boji. Njegov izgled je prikazan na slici 3.

NaH ima molekulsku masu od 23.99771 g / mol, gustoću od 1.396 g / ml i točku tališta od 800 ° C (Royal Society of Chemistry, 2015). Nije topiv u amonijaku, benzenu, ugljikovom tetrakloridu i ugljikovom disulfidu (Nacionalni centar za biotehnološke informacije, s.f.).
Spoj je izrazito nestabilan. Čisti NaH lako se može zapaliti u zraku. Kada dođe u dodir s vodom koja je prisutna u zraku, oslobađa vrlo zapaljiv vodik.
Kada je otvoren za zrak i vlagu, NaH se također lako hidrolizira u jaku korozivnu bazu natrijevog hidroksida (NaOH) prema reakciji:
NaH + H20 → NaOH + H2
U ovoj reakciji može se uočiti da se natrijev hidrid ponaša kao baza. To je zbog elektronegativnosti.
Natrij ima znatno nižu elektronegativnost (≈1.0) od vodika (≈2.1), što znači da vodik ekstrahira gustoću elektrona prema sebi, udaljavajući se od natrija kako bi generirao natrijev kation i anion. hidrida.
Da bi spoj bio Brønstedova kiselina, treba razdvojiti elektronsku gustoću od vodika, to jest, povezati ga s elektronegativnim atomom kao što je kisik, fluor, dušik itd. Tek tada se može formalno opisati kao H + i može se disocirati kao takva.
Hidrid je mnogo bolje opisan kao H- i ima slobodan par elektrona. Kao takav, to je Brønstedova baza, a ne kiselina. Zapravo, ako proširimo definiciju Brønstedove kiseline i baze na način na koji je to učinio Lewis, doći ćete do zaključka da je natrij (Na +) ovdje kiselinska vrsta.
Brønstedov produkt reakcije kiseline / baze H-baze i H + kiselina postaje H2. Budući da se kiseli vodik ekstrahira izravno iz vode, plin vodik se može miješati, premještajući ravnotežu čak i ako reakcija nije termodinamički pogodna.
Može se ostaviti OH-ioni koji se mogu zapisati s ostatkom Na + kationa kako bi se dobio natrijev hidroksid (Zašto je čvrsti natrijev hidrid, a ne kiselina kad reagira s vodom?, 2016).
Reaktivnost i opasnosti
Spoj je snažno redukcijsko sredstvo. Napada SiO2 u staklu. Pali se pri kontaktu s plinovitim F2, Cl2, Br2 i I2 (potonji na temperaturama iznad 100 ° C), posebno u prisutnosti vlage, da bi se formirali HF, HCl, HBr i HI.
Reagira sa sumporom dajući Na2S i H2S. Može eksplozivno reagirati s dimetil sulfoksidom. Reagira snažno s acetilenom, čak i na -60 ° C. Spontano je zapaljiv u fluoru.
Inicira reakciju polimerizacije u etil-2,2,3-trifluoropropionatu, tako da se ester snažno razgrađuje. Prisutnost u reakciji dietil sukcinata i etil trifluoroacetata izazvala je eksplozije (SODIUM HYDRIDE, 2016).
Natrijev hidrid se smatra korozivnim za kožu ili oči, zbog potencijala kaustičnih nusprodukata reakcija s vodom.
U slučaju kontakta s očima, treba ih isprati s velikom količinom vode, ispod kapaka najmanje 15 minuta i odmah potražiti liječničku pomoć..
U slučaju dodira s kožom, odmah očistite i isperite zahvaćeno područje vodom. Ako iritacija ne prestane, potražite liječničku pomoć.
Štetan je zbog gutanja uslijed reakcije na vodu. Ne izazivati povraćanje. Odmah potražite liječničku pomoć i prebacite žrtvu u medicinski centar.
Disperzija natrijevog hidrida u ulju nije prašina. Međutim, materijal koji reagira može emitirati finu kaustičnu maglu. U slučaju udisanja, isprati usta vodom i prebaciti žrtvu na mjesto sa svježim zrakom. Treba tražiti medicinsku pomoć (Rhom i Hass Inc., 2007).
aplikacije
Glavna primjena natrijevog hidrida je izvođenje kondenzacijskih i alkilacijskih reakcija koje nastaju stvaranjem karbaniona (kataliziranog bazom)..
Natrijev hidrid u ulju podsjeća na natrijeve i natrijeve metalne alkoholate, u svojoj sposobnosti da djeluje kao sredstvo za deprotoniranje u acetoacetičnom esteru, Claisen, Stobbe, Dieckmann i druge srodne reakcije. To je pokazalo prednosti u odnosu na druge kondenzacijske agense u tome:
- To je jača baza, što rezultira izravnijom deprotonacijom.
- Nikakav višak nije potreban.
- Dobiveni H2 daje mjeru opsega reakcije.
- Sekundarne reakcije kao što su redukcije su eliminirane.
Alkilacije aromatskih i heterocikličkih amina kao što su 2-aminopiridin i fenotiazin lako se postižu pri visokom prinosu koristeći smjese toluen-metilformamida. Koncentracija dimetilformamida je varijabla koja se koristi za kontrolu brzine reakcije (HINCKLEY, 1957).
Predložena je upotreba natrijevog hidrida za skladištenje vodika za upotrebu u vozilima s gorivim ćelijama, pri čemu je hidrid zatvoren u plastične granule koje su smrvljene u prisutnosti vode za oslobađanje vodika.
reference
- HINCKLEY, M.D. (1957). Proizvodnja, rukovanje i uporaba natrijevog hidrida. Advances in Chemistry, svezak 19, 106-117.
- Mark Winter [Sveučilište u Sheffieldu i WebElements Ltd, U. (1993.-2016.). Natrij: natrijev hidrid. Preuzeto s WebElements: webelements.com.
- Nacionalni centar za biotehnološke informacije. (N. D.). PubChem Compound Database; CID = 24758. Preuzeto iz PubChem: pubchem.ncbi.nlm.nih.gov.
- Rhom i Hass inc. (2007, prosinac). Natrijev hidrid 60% disperzija u ulju. Preuzeto s web-lokacije dow.com.
- Kraljevsko kemijsko društvo. (2015). Natrijev hidrid. Preuzeto iz ChemSpider: chemspider.com.
- Natrijev hidrid. (2016). Preuzeto iz cameochemicals: cameochemicals.noaa.gov.
- Formula natrij hidrida - upotreba, svojstva, struktura i formula natrijeva hidrida. (2005-2017). Dobavljeno iz Softschools.com: softschools.com.
- Natrijev hidrid. (N. D.). Preuzeto iz kemijskih proizvoda21: chemicalland21.com.
- Zašto je čvrsti natrijev hidrid, a ne kiselina kada reagira s vodom? (2016., 20. travnja). Dobavljeno iz stackexchange: chemistry.stackexchange.com.


