Struktura amonijevog hidroksida, svojstva, nomenklatura, uporaba
amonij hidroksid R3 je spoj NH molekulske formule4OH ili H5NE proizvodi se otapanjem plinovitog amonijaka (NH3) u vodi. Iz tog razloga dobiva imena amonijačne vode ili tekućeg amonijaka.
To je bezbojna tekućina vrlo intenzivnog i oštrog mirisa, koja nije izolacijska. Ove karakteristike imaju izravnu vezu s koncentracijom NH3 otopljen u vodi; Koncentracija koja je zapravo plin, može pokriti velike količine otopljene u maloj količini vode.
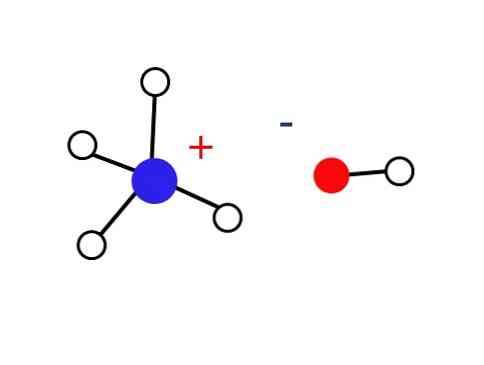
Znatno mali dio ovih vodenih otopina sastoji se od NH kationa4+ i OH aniona-. S druge strane, u vrlo razrijeđenim otopinama ili u smrznutoj krutini pri vrlo niskim temperaturama amonijak se može naći u obliku hidrata, kao što su: NH3H2O, 2NH3H2O i NH32H2O.
Kao neobična činjenica, Jupiterovi oblaci nastaju razrijeđenim otopinama amonijevog hidroksida. Međutim, svemirska sonda Galilea nije uspjela pronaći vodu u oblacima planeta, što bi se moglo očekivati iz spoznaje da je poznato stvaranje amonijevog hidroksida; to su NH kristali4OH potpuno bezvodni.
Amonijev ion (NH4+) stvara se u lumenu tubularnog crijeva preko spoja amonijaka i vodika, kojeg luče tubularne stanice bubrega. Isto tako, amonij se proizvodi u tubularnim stanicama bubrega u procesu pretvorbe glutamina u glutamat, a zatim, u pretvorbi glutamata u a-ketoglutarat..
Amonijak se industrijski proizvodi Haber-Bosch metodom, u kojoj reagiraju plinovi dušika i vodika; upotrebom željeznog iona, aluminijevog oksida i kalijevog oksida kao katalizatora. Reakcija se provodi pri visokim tlakovima (150 - 300 atmosfera) i visokim temperaturama (400-500 ºC), uz prinos od 10-20%..
U reakciji se proizvodi amonijak koji, kada se oksidira, proizvodi nitrite i nitrate. To je neophodno za dobivanje dušične kiseline i gnojiva kao što je amonijev nitrat.
indeks
- 1 Kemijska struktura
- 1.1 Amonijačni led
- 2 Fizikalna i kemijska svojstva
- 2.1 Molekularna formula
- 2.2 Molekularna težina
- 2.3 Izgled
- 2.4 Koncentracija
- 2.5 Miris
- 2.6 Okus
- 2.7 Vrijednost praga
- 2.8 Vrelište
- 2.9 Topljivost
- 2.10 Topljivost u vodi
- 2.11 Gustoća
- 2.12 Gustoća pare
- 2.13 Tlak pare
- 2.14 Korozivno djelovanje
- 2,15 pH
- 2.16 Konstanta disocijacije
- 3 Nomenklatura
- 4 Topljivost
- 5 Rizici
- 5.1 Reaktivnost
- 6 Upotreba
- 6.1 U hrani
- 6.2. Terapeutici
- 6.3 Industrijski i razni
- 6.4 U poljoprivredi
- 7 Reference
Kemijska struktura
Kao što pokazuje njegova definicija, amonijev hidroksid se sastoji od vodene otopine plina amonijaka. Prema tome, unutar tekućine ne postoji drugačija struktura od slučajnog rasporeda NH iona4+ i OH- solvatirane molekulama vode.
Amonijevi i hidroksilni ioni su produkti ravnoteže hidrolize amonijaka, pa je uobičajeno da ta otopina ima oštar miris:
NH3(g) + H2O (l) <=> NH4+(ac) + OH-(Aq)
Prema kemijskoj jednadžbi, veliko smanjenje koncentracije vode bi pomaklo ravnotežu na stvaranje više amonijaka; to jest, dok se amonijev hidroksid zagrijava, ispuštaju se para amonijaka.
Iz tog razloga, NH ioni4+ i OH- ne uspijevaju formirati kristal u zemaljskim uvjetima, što dovodi do posljedica da čvrsta baza NH4OH ne postoji.
Ova kruta tvar treba biti sastavljena samo od iona koji su interaktivni elektrostatički (kao što je prikazano na slici).
Amonijačni led
Međutim, pod temperaturama ispod 0ºC i okružene ogromnim pritiscima, kao što su oni koji prevladavaju u jezgri ledenih mjeseca, smrzavaju se amonijak i voda. Pri tome kristaliziraju u krutoj smjesi s različitim stehiometrijskim razmjerima, što je najjednostavniji NH3H2O: amonijak monohidrat.
NH3H2O i NH32H2Ili su amonijačni led, jer se kruta tvar sastoji od kristalnog rasporeda molekula vode i amonijaka spojenog vodikovim vezama..
S obzirom na promjenu T i P, prema računalnim studijama koje simuliraju sve fizikalne varijable i njihove učinke na ovaj led, dolazi do prijelaza NH faze3. NH2Ili u NH fazu4OH.
Stoga, samo u tim ekstremnim uvjetima, NH4OH može postojati kao produkt protonacije unutar leda između NH3 i H2O:
NH3(s) + H2O (s) <=> NH4OH (s)
Imajte na umu da su, za razliku od hidrolize amonijaka, uključene vrste u čvrstoj fazi. Amonijačni led koji postaje slan bez otpuštanja amonijaka.
Fizikalna i kemijska svojstva
Molekularna formula
NH4OH ili H5NE
Molekularna težina
35,046 g / mol
izgled
To je bezbojna tekućina.
koncentracija
Do približno 30% (za NH ione4+ i OH-).
miris
Vrlo jaka i oštra.
aroma
ral.
Vrijednost praga
34 ppm za nespecifično otkrivanje.
Točka vrenja
38 ºC (25%).
topljivost
Postoji samo u vodenoj otopini.
Topljivost u vodi
Može se miješati u neograničenim razmjerima.
gustoća
0,90 g / cm3 na 25 ° C.
Gustoća pare
U odnosu na zrak koji se uzima kao jedinica: 0.6. To jest, manje je gust od zraka. Međutim, logično, prijavljena vrijednost odnosi se na amonijak kao plin, a ne na njegove vodene otopine ili na NH4OH.
Tlak pare
2.160 mmHg na 25 ° C.
Nagrizajuće djelovanje
Sposoban je otapati cink i bakar.
pH
11,6 (otopina 1 N); 11.1 (otopina 0.1 N) i 10,6 (0,01 N otopina).
Konstanta disocijacije
pKb = 4,767; Kb = 1,71 x 10-5 na 20 ° C
pKb = 4,751; Kb = 1,774 x 10-5 na 25 ° C.
Povećanje temperature gotovo neprimjetno povećava bazičnost amonijevog hidroksida.
nomenklatura
Koja su sve uobičajena i službena imena koja NH dobiva?4OH? Prema onome što je utvrdio IUPAC, ime mu je amonijev hidroksid jer sadrži hidroksil anion.
Amonij po svom opterećenju +1 je monovalentan, zbog razloga što se upotrebom nomenklature Zalihe naziva: amonijev hidroksid (I).
Iako je upotreba izraza amonijev hidroksid tehnički netočna, budući da se spoj ne može izolirati (barem ne na Zemlji, kako je detaljno objašnjeno u prvom odjeljku).
Osim toga, amonijev hidroksid dobiva nazive amonijačne vode i tekućeg amonijaka.
topljivost
NH4OH, budući da nema soli u zemaljskim uvjetima, ne može se procijeniti koliko je topljiva u različitim otapalima.
Međutim, moglo bi se očekivati da bude iznimno topiv u vodi, jer bi njegovo otapanje oslobodilo velike količine NH3. Teoretski, to bi bio nevjerojatan način skladištenja i transporta amonijaka.
U drugim otapalima sposobnim za prihvaćanje vodikovih veza, kao što su alkoholi i amini, može se očekivati da će također biti vrlo topljiva u njima. Ovdje NH kation4+ je donor vodikovih mostova i OH- radi kao oboje.
Primjeri ovih interakcija s metanolom bili bi: H3N+-H-OHCH3 i HO- - HOCH3 (OHCH3 pokazuje da kisik prima vodikovu vezu, a ne da je metil grupa povezana s H).
rizici
-U kontaktu s očima uzrokuje iritaciju koja može dovesti do oštećenja očiju.
-To je nagrizajuće. Stoga, u dodiru s kožom može uzrokovati iritaciju i pri visokim koncentracijama reagensa, uzrokovati opekline kože. Ponovljeni kontakt amonijevog hidroksida s kožom može uzrokovati njegovu suhoću, svrbež i crvenilo (dermatitis)..
-Udisanje spreja amonijevog hidroksida može uzrokovati akutnu iritaciju respiratornog trakta, koju karakterizira gušenje, kašljanje ili kratak dah. Dugotrajno ili ponavljano izlaganje tvari može rezultirati povratnim bronhijalnim infekcijama. Također, udisanje amonijevog hidroksida može uzrokovati iritaciju pluća.
-Izloženost visokim koncentracijama amonijevog hidroksida može biti hitna medicinska pomoć, jer se može pojaviti nakupljanje tekućine u plućima (plućni edem)..
-Koncentracija od 25 ppm uzeta je kao granica izloženosti, u 8-satnoj radnoj smjeni, u okruženju u kojem je radnik izložen štetnom djelovanju amonijevog hidroksida.
reaktivnost
-Osim toga, potencijalne štete po zdravlje izložene amonijevom hidroksidu, postoje i druge mjere opreza koje se moraju uzeti u obzir pri radu s tvari.
-Amonijev hidroksid može reagirati s mnogim metalima, kao što su: srebro, bakar, olovo i cink. On također reagira sa solima tih metala u obliku eksplozivnih spojeva i oslobađa plinoviti vodik; koji je pak zapaljiv i eksplozivan.
-Može burno reagirati s jakim kiselinama, primjerice klorovodičnom kiselinom, sumpornom kiselinom i dušičnom kiselinom. Isto tako, on reagira na isti način s dimetil sulfatom i halogenima.
-Reagira s jakim bazama, kao što su natrijev hidroksid i kalijev hidroksid, proizvodeći plinoviti amonijak. To se može provjeriti ako se promatra ravnoteža u otopini, u kojoj se dodaju OH ioni- prebacuje ravnotežu na stvaranje NH3.
-Bakreni i aluminijski metali, kao i drugi galvanizirani metali, ne smiju se koristiti pri rukovanju amonijevim hidroksidom zbog korozivnog djelovanja na njih..
aplikacije
U hrani
-Koristi se kao dodatak u mnogim namirnicama u kojima djeluje kao agens za kvasac, pH kontrolni i završni agens površine hrane..
-Popis namirnica u kojima se koristi amonijev hidroksid je opsežan i uključuje pečene proizvode, sireve, čokolade, bombone i pudinge.
-FDA je klasificirala amonijev hidroksid kao sigurnu tvar za preradu hrane, pod uvjetom da se poštuju utvrđeni standardi.
-U mesnim proizvodima koristi se kao antimikrobni agens, koji može eliminirati bakterije kao što je E. coli, reducirajući ih na nedetektabilne razine. Bakterija se nalazi u crijevima goveda, prilagođavajući se kiselom okolišu. Amonijev hidroksid, regulirajući pH, sprečava rast bakterija.
terapeutski
-Amonijev hidroksid ima nekoliko terapijskih primjena, uključujući:
-10% otopina se koristi kao stimulans respiratornog refleksa
-Izvana se koristi na koži za liječenje ujeda i ugriza kukaca - Djeluje na probavni sustav kao antacid i karminativ, odnosno pomaže eliminaciju plinova.
Osim toga, koristi se kao topikalni rubefacient za akutnu i kroničnu muskuloskeletnu bol. Kao posljedica rubefacijantnog djelovanja amonijevog hidroksida, lokalno se povećava protok krvi, crvenilo i iritacija.
Industrijski i razni
-Djeluje u smanjenju NOx (visoko reaktivni plinovi kao što je dušikov oksid (NO) i dušikov dioksid (NO.)2)) za emisije dimnih plinova i smanjenje NOx u emisijama dimnjaka.
-Koristi se kao sredstvo za plastificiranje; Aditiv boja i obrada površina.
-Povećava poroznost kose omogućujući pigmentima mrlja da imaju veću penetraciju, čime se postiže bolja završna obrada..
-Amonijev hidroksid se koristi kao antimikrobno sredstvo u obradi otpadnih voda. Osim toga, ona intervenira u sintezi kloramina. Ova tvar ispunjava funkciju sličnu kloru u pročišćavanju vode u bazenima, koja ima prednost što je manje toksična.
-Koristi se kao inhibitor korozije u procesu rafiniranja ulja.
-Koristi se kao sredstvo za čišćenje u raznim industrijskim i komercijalnim proizvodima, a koristi se na više površina, uključujući: nehrđajući čelik, porculan, staklo i pećnicu.
-Osim toga, koristi se u proizvodnji deterdženata, sapuna, lijekova i tinti.
U poljoprivredi
Iako se ne daje izravno kao gnojivo, amonijev hidroksid ispunjava tu funkciju. Amonijak se proizvodi iz atmosferskog dušika Haber-Bosch metodom i transportira u hladnjaku ispod točke vrelišta (-33 ° C) do mjesta njegova korištenja.
Stlačeni amonijak se injektira u obliku pare u tlo gdje odmah reagira s edafskom vodom i prelazi u amonijev oblik (NH)4+), koji se zadržava u mjestima izmjene kationa tla. Dodatno se proizvodi amonijev hidroksid. Ovi spojevi su izvor dušika.
Zajedno s fosforom i kalijem, dušik čini triju glavnih hranjivih tvari biljaka neophodnih za njegov rast.
reference
- Ganong, W. F. (2002.) Medicinska fiziologija. 19. izdanje. Uvodnik Moderni priručnik.
- A. D. Fortes, J. P. Brodholt, I. G. Wood i L. Vocadlo. (2001). Ab initio simulacija amonijaka monohidrata (NH3H2O) i amonijev hidroksid (NH4OH). Američki institut za fiziku. J. Chem., Phys., Svezak 115, br. 15, 15.
- Helmenstine, Anne Marie, Ph.D. (6. veljače 2017.) Činjenice o amonijevom hidroksidu. Preuzeto s: thoughtco.com
- Grupa Pochteca. (2015). Amonijev hidroksid. pochteca.com.mx
- NJ Health (N. D.). Podaci o opasnim tvarima: amonijev hidroksid. [PDF]. Preuzeto s: nj.gov
- Polaznik kemije. (2018.). Amonijev hidroksid. Preuzeto s: chemistrylearner.com
- Pubchem. (2018.). Amonijev hidroksid. Preuzeto s: pubchem.ncbi.nlm.nih.gov


