Postupak egzotermne reakcije, tipovi i primjeri
egzotermna reakcija je vrsta kemijske reakcije u kojoj dolazi do prijenosa energije, uglavnom u obliku oslobađanja topline ili svjetla. Ime dolazi od grčkog prefiksa exo, što znači "u inozemstvu"; i izraz "toplinski", koji se odnosi na toplinu ili temperaturu.
U tom smislu, egzotermne reakcije mogu prenijeti druge vrste energije u okolinu u kojoj nastaju, kao što su eksplozije i njihov način prijenosa kinetičke i zvučne energije kada se tvari koje su u plinovitoj fazi pri visokim temperaturama proširuju. nasilan način.
Na isti način, u slučaju uporabe baterija, provodi se egzotermna reakcija, samo u ovom slučaju se prenosi električna energija.
indeks
- 1 Proces
- 2 Vrste
- 2.1 Reakcije izgaranja
- 2.2 Neutralizacijske reakcije
- 2.3 Reakcije oksidacije
- 2.4 Reakcija termita
- 2.5 Reakcijska polimerizacija
- 2.6 Reakcija nuklearne fisije
- 2.7 Ostale reakcije
- 3 Primjeri
- 4 Reference
proces
Prethodno je spomenuto da kada dođe do egzotermne reakcije dolazi do oslobađanja energije, što se može lakše vizualizirati u sljedećoj jednadžbi:
Reagensi → Proizvod (i) + Energija
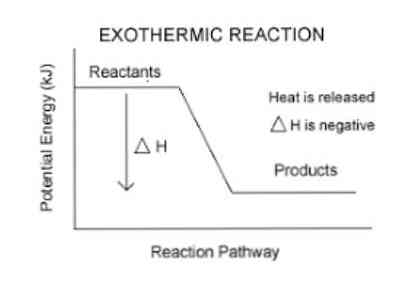
Dakle, za kvantificiranje energije koja je apsorbirana ili oslobođena od strane sustava, koristi se termodinamički parametar koji se naziva entalpija (označena s "H"). Ako u sustavu (u ovom slučaju kemijskoj reakciji) dolazi do oslobađanja energije u okolinu, tada će varijacija entalpije (izražena kao ΔH) imati negativnu vrijednost.
Inače, ako je varijacija ove mjere pozitivna, ona odražava apsorpciju topline iz okoline. Također, veličina varijacije entalpije sustava je izraz količine energije koja se prenosi u ili iz okoline.
Što je veća veličina ΔH, to je veće oslobađanje energije iz sustava u okolni medij.
To je zbog toga što je u tim reakcijama neto energija koja se oslobađa pri stvaranju novih veza veća od neto energije koja se koristi u fragmentaciji veza.
Iz navedenog može se zaključiti da je ova vrsta reakcija vrlo česta, jer proizvodi reakcije imaju količinu energije pohranjene u vezama koja je veća od one sadržane u reaktantima..
vrsta
Postoje različite vrste egzotermnih reakcija u različitim područjima kemije, bilo u laboratoriju ili u industriji; neke se spontano izvode, a drugima su potrebni specifični uvjeti ili neka vrsta tvari kao što je katalizator.
Sljedeće su najvažnije vrste egzotermnih reakcija:
Reakcije izgaranja
Reakcije izgaranja su one koje imaju redox tip koji se javljaju kada jedna ili više tvari reagira s kisikom, što općenito rezultira oslobađanjem svjetlosti i toplinske energije - to jest, svjetlo i toplina - kada se plamen proizvodi..
Reakcije neutralizacije
Neutralizacijske reakcije karakterizira interakcija između kiselinskih vrsta i alkalnih tvari (baza) kako bi se formirala sol i voda, što pokazuje egzotermičku prirodu..
Reakcije oksidacije
Postoje mnoge reakcije ovog tipa koje pokazuju egzotermno ponašanje, jer oksidacija kisika uzrokuje oslobađanje velike količine energije, kao što se događa u oksidaciji ugljikovodika..
Reakcija termita
Ova reakcija može proizvesti temperaturu od približno 3000 ° C, a zbog visokog afiniteta aluminijskog praha s velikim brojem metalnih oksida, koristi se za zavarivanje čelika i željeza..
Reakcija polimerizacije
Ovaj tip reakcije je onaj koji nastaje kada određeni broj kemijskih vrsta koje se nazivaju monomeri reagira, što su jedinice koje se u kombinaciji ponavljaju u lancima i tvore makromolekularne strukture zvane polimeri.
Reakcija nuklearne fisije
Taj se proces odnosi na podjelu nukleusa atoma koji se smatra teškim - to jest, s masenim brojem (A) većim od 200 - da se dobiju fragmenti ili jezgre manje veličine s srednjom masom.
U ovoj reakciji, gdje nastaje jedan ili više neutrona, oslobađa se velika količina energije jer jezgra s većom težinom ima manju stabilnost od svojih proizvoda.
Ostale reakcije
Postoje i druge egzotermne reakcije od velike važnosti, kao što je dehidracija nekih ugljikohidrata pri reakciji sa sumpornom kiselinom, apsorpcija vode koja je izložena natrij hidroksidu na otvorenom ili oksidacija metalnih vrsta u mnogim reakcijama korozije..
Primjeri
U nastavku su navedeni neki primjeri egzotermnih reakcija, koje proizvode varijaciju entalpije koja ima negativnu vrijednost zbog činjenice da oslobađaju energiju, kao što je gore spomenuto..
Na primjer, izgaranje propana je spontana egzotermna reakcija:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Drugi slučaj egzotermnog ponašanja pokazuje reakcija neutralizacije između natrijevog karbonata i klorovodične kiseline:
ot.3(ac) + HCl (ac) - NaCl (ac) + H2O (1) + CO2(G)
Prikazana je i oksidacija etanola u octenu kiselinu koja se koristi u analizatorima, čija je kompletna reakcija prikazana u sljedećoj jednadžbi:
3CH3CH2OH + 2K2Cr2O7 + 8H2SW4 → CH3COOH + 2Cr (SO4)3 + 2K2SW4 + 11H2O
Druga klasa egzotermne reakcije je tzv. Termitna reakcija, u kojoj se aluminij kombinira s metalnim oksidom, kao što je prikazano niže:
2Al (s) + vjera2O3(s) → Al2O3(s) + Fe (l)
Osim gore objašnjenih primjera, postoji širok raspon reakcija koje se također smatraju egzotermičkim, kao što je razgradnja određenih organskih otpadnih tvari za kompostiranje..
Također ističe oksidaciju luciferinskog pigmenta djelovanjem enzima luciferaze kako bi se proizvela bioluminiscencija karakteristična za krijesnice, pa čak i disanje, među mnogim drugim reakcijama.
reference
- Wikipedia. (N. D.). Egzotermna reakcija. Preuzeto s es.wikipedia.org
- BBC. (N. D.). Energetske promjene i reverzibilne reakcije. Preuzeto s bbc.co.uk
- Chang, R. (2007). Kemija, 9. izdanje. (McGraw-Hill).
- Walker, D. (2007). Kemijske reakcije. Preuzeto s books.google.co.ve
- Saunders, N. (2007). Istraživanje kemijskih reakcija. Preuzeto s books.google.co.ve


