Struktura, svojstva, nomenklatura i upotreba srebrovog oksida (Ag2O)
srebrni oksid je anorganski spoj čija je kemijska formula Ag2O. Sila koja spaja njegove atome je potpuno ionske prirode; dakle, on se sastoji od ionske krutine u kojoj postoji omjer dva Ag kationa+ interakcija elektrostatički s anionom O2-.
Anion oksida, O2-, rezultat je interakcije atoma srebra površine s kisikom okoline; na vrlo sličan način željeza i mnogih drugih metala. Srebrni komad ili nakit umjesto crvenila i rušenja, postaje crn, karakterističan za srebrni oksid.

Na primjer, na gornjoj slici možete vidjeti zahrđalu srebrnu čašu. Zabilježite njezinu pocrnjenu površinu, iako i dalje zadržava neki ukrasni sjaj; zbog čega se čak i zarđali predmeti od srebra mogu smatrati dovoljno privlačnim za dekorativne namjene.
Svojstva srebrnog oksida su takva da na prvi pogled ne kvare izvornu metalnu površinu. Formira se na sobnoj temperaturi jednostavnim kontaktom s kisikom u zraku; i još zanimljivije, može se raspasti pri visokim temperaturama (iznad 200 ° C).
To znači da bi, ako bi se držalo staklo slike, a toplina intenzivnog plamena bila primijenjena, povratila svoj srebrni sjaj. Stoga je njegovo formiranje termodinamički reverzibilni proces.
Srebrni oksid također ima druga svojstva i, izvan svoje jednostavne Ag formule2Ili obuhvaća složene strukturne organizacije i bogatu raznolikost krutih tijela. Međutim, Ag2Ili je možda, uz Ag2O3, najreprezentativniji od oksida srebra.
indeks
- 1 Struktura srebrnog oksida
- 1.1 Promjene s brojem valencije
- 2 Fizikalna i kemijska svojstva
- 2.1 Molekularna težina
- 2.2 Izgled
- 2.3 Gustoća
- 2.4 Točka taljenja
- 2,5 Kps
- 2.6 Topljivost
- 2.7 Kovalentni znak
- 2.8 Raspadanje
- 3 Nomenklatura
- 3.1 Valencias I i III
- 3.2. Sustavna nomenklatura za složene srebrove okside
- 4 Upotreba
- 5 Reference
Struktura srebrnog oksida
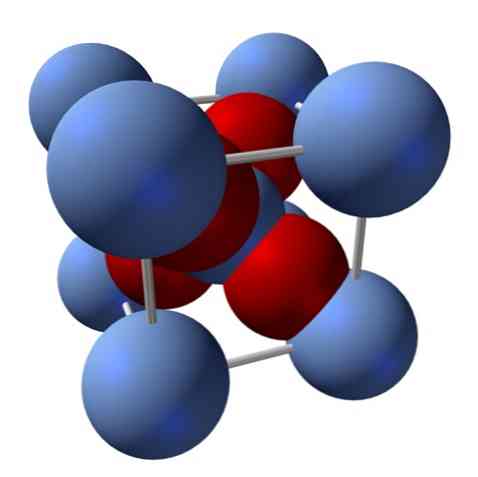
Kako je njegova struktura? Kao što je spomenuto na početku: to je ionska krutina. Zbog toga u njegovoj strukturi ne mogu postojati kovalentne veze Ag - O niti Ag = O; budući da bi, ako bi postojala, svojstva tog oksida drastično promijenila. Tada su Ag ioni+ i O2- u omjeru 2: 1 i doživljava elektrostatičku privlačnost.
Struktura srebrnog oksida određena je posljedicom načina na koji ionske sile odlažu u prostor Ag ione+ i O2-.
Na gornjoj slici, na primjer, imate jediničnu ćeliju za kubični kristalni sustav: Ag katione+ su srebrno plave kugle i O2- crvenkaste kugle.
Ako brojite sfere, otkrit ćete da na prvi pogled ima devet srebrno plavih i četiri crvene boje. Međutim, uzimaju se u obzir samo fragmenti sfera sadržanih u kocki; da bi se brojali ovi, kao dijelovi ukupnih sfera, mora biti zadovoljen omjer 2: 1 za Ag2O.
Ponavljanje strukturne jedinice tetraedra AgO4 okružen s još četiri Ag+, izgrađena je sva crna krutina (otklanjanje praznina ili nepravilnosti koje ti kristalni aranžmani mogu imati).
Mijenja se s brojem valencije
Fokusiranje sada nije na AgO tetraedar4 ali u liniji AgOAg (promatrati vrhove gornje kocke), krutina srebrnog oksida sastoji se, iz druge perspektive, od višestrukih ionskih slojeva raspoređenih linearno (iako nagnutih). Sve to kao rezultat "molekularne" geometrije oko Ag+.
Navedeno je potkrijepljeno nekoliko istraživanja njezine ionske strukture.
Srebro djeluje pretežno s valencijom +1, jer pri gubljenju elektrona njegova elektronička konfiguracija je [Kr] 4d10, koja je vrlo stabilna. Ostale valencije, kao što je Ag2+ i Ag3+ one su manje stabilne jer gube elektrone iz orbitala gotovo u potpunosti ispunjene.
Agon3+, međutim, ona je relativno manje nestabilna u usporedbi s Ag2+. Zapravo, može postojati u društvu Ag+ Kemijski obogaćujući strukturu.
Njegova elektronička konfiguracija je [Kr] 4d8, s nesparenim elektronima na takav način da mu daje neku stabilnost.
Za razliku od linearnih geometrija oko Ag iona+, Ustanovljeno je da su Ag ioni3+ To je kvadratni stan. Stoga, srebrov oksid s Ag ionima3+ sastojala bi se od slojeva sastavljenih od AgO kvadrata4 (ne tetraedre) elektrostatički povezane AgOAg linijama; Takav je slučaj Ag4O4 ili Ag2O. Ag2O3 s monoklinskom strukturom.
Fizikalna i kemijska svojstva

Ako zagrebete površinu srebrne čaše glavne slike, dobili biste čvrstu, koja nije samo crna, već i smeđe ili smeđe boje (gornja slika). Neke od njegovih fizikalnih i kemijskih svojstava opisanih u trenucima su sljedeće:
Molekularna težina
231,735 g / mol
izgled
Čvrsto crno smeđe u obliku praha (imajte na umu da unatoč tome što je ionska krutina nema kristalni izgled). Bez mirisa je i pomiješan s vodom daje metalni okus
gustoća
7,14 g / ml.
Točka taljenja
277-300 ° C. Zasigurno se topi u čvrsto srebro; to jest, vjerojatno se razgrađuje prije formiranja tekućeg oksida.
KPS
1,52. 10-8 u vodi na 20 ° C. Zbog toga je spoj jedva topiv u vodi.
topljivost
Ako pažljivo pogledate sliku njezine strukture vidjet ćete da su sfere Ag2+ i O2- Ne razlikuju se gotovo po veličini. Kao rezultat, samo male molekule mogu prodrijeti u unutrašnjost kristalne rešetke, što je čini netopljivom u gotovo svim otapalima; osim onih u kojima reagira, kao što su baze i kiseline.
Kovalentni znak
Iako je više puta rečeno da je srebrni oksid ionski spoj, određena svojstva, kao što je niska točka taljenja, u suprotnosti su s ovom tvrdnjom..
Svakako, razmatranje kovalentnog karaktera ne razbija ono što je objašnjeno za njegovu strukturu, bilo bi dovoljno dodati ga strukturi Ag.2Ili model sfera i šipki za označavanje kovalentnih veza.
Također, tetraedre i kvadratne ravnine AgO4, kao i AgOAg linije, one bi bile povezane kovalentnim (ili kovalentnim ionskim) vezama.
S tim na umu, Ag2Ili bi zapravo bio polimer. Međutim, preporuča se promatrati ga kao ionsku krutinu s kovalentnim karakterom (čija je priroda veze još uvijek izazov).
raspad
U početku je spomenuto da je njegovo formiranje termodinamički reverzibilno, tako da apsorbira toplinu da se vrati u svoje metalno stanje. Sve se to može izraziti s dvije kemijske jednadžbe za takve reakcije:
4Ag (s) + 02(g) => 2Ag2O (s) + Q
2AG2O (s) + Q => 4Ag (s) + O2(G)
Gdje Q predstavlja toplinu u jednadžbi. To objašnjava zašto vatra koja gori na površini zahrđale srebrne čaše vraća svoj srebrni sjaj.
Stoga je teško pretpostaviti da postoji Ag2O (l) jer bi se odmah raspadalo toplinom; osim ako je tlak previsok za dobivanje te smeđe crne tekućine.
nomenklatura
Kada je uvedena mogućnost Ag iona2+ i Ag3+ osim zajedničkog i prevladavajućeg Ag+, pojam 'srebrni oksid' počinje se činiti nedovoljnim da bi se odnosio na Ag2O.
To je zato što Ag+ više je od drugih, tako da se uzima Ag2Ili kao jedini oksid; što uopće nije točno.
Ako uzmete u obzir Ag2+ kao praktički nepostojeći s obzirom na njegovu nestabilnost, tada će biti prisutni samo ioni s valencijama +1 i +3; to jest, Ag (I) i Ag (III).
Valencias I i III
Budući da je Ag (I) najmanje valencija, naziva se dodavanjem sufiksa -oso u njegovo ime Argentum. Dakle, Ag2Ili je to: argentoso oksid ili, prema sustavnoj nomenklaturi, diplata monoksid.
Ako je Ag (III) potpuno zanemaren, tada njegova tradicionalna nomenklatura mora biti: srebrov oksid umjesto argentinskog oksida.
S druge strane, Ag (III) kao veća valencija dodaje se sufiksu -ico u njegovo ime. Dakle, Ag2O3 je: srebrov oksid (2 Ag ioni)3+ s tri O2-). Također, njegovo bi ime prema sustavnoj nomenklaturi bilo: diploma trioksid.
Ako se promatra struktura Ag2O3, može se pretpostaviti da je to proizvod oksidacije ozonom, OR3, umjesto kisika. Stoga, njegov kovalentni karakter mora biti veći jer je kovalentni spoj s Ag-O-O-O-Ag ili Ag-O vezama.3-Ag.
Sustavna nomenklatura za složene srebrove okside
AgO, također napisan kao Ag4O4 ili Ag2O. Ag2O3, to je srebrni oksid (I, III), budući da ima obje valencije +1 i +3. Njegovo ime prema sustavnoj nomenklaturi bilo bi: tetraplate tetraoksid.
Ova nomenklatura je od velike pomoći kada se radi o drugim stehiometrijski složenijim srebrnim oksidima. Na primjer, pretpostavimo dvije krute tvari 2Ag2O. Ag2O3 i Ag2O '3Ag2O3.
Pisanje prvog na prikladniji način bilo bi: Ag6O5 (brojanje i dodavanje atoma Ag i O). Njegovo ime bi onda bio heksaplat pentoksid. Treba napomenuti da ovaj oksid ima srebreni sastav manje bogat od Ag2O (6: 5) < 2:1).
Inače bi drugo pisanje bilo: Ag8O10. Njegovo ime bi bilo oktaplat decaoxide (s omjerom 8:10 ili 4: 5). Ovaj hipotetski srebrni oksid bio bi "vrlo oksidiran".
aplikacije
Još se danas provode istraživanja u potrazi za novim i sofisticiranim uporabama srebrnog oksida. Neke od njegovih uporaba navedene su u nastavku:
-Otopi se u amonijaku, amonijevom nitratu i vodi da se dobije Tollens reagens. Ovaj reagens je koristan alat u kvalitativnim analizama u laboratorijima organske kemije. Omogućuje određivanje prisutnosti aldehida u uzorku, a pozitivan odgovor je stvaranje "srebrnog ogledala" u epruveti.
-Zajedno s metalnim cinkom tvori primarne baterije cinkovog oksida srebra. To je možda jedna od najčešćih i najčešćih uporaba.
-Služi kao pročišćivač plina, apsorbirajući na primjer CO2. Kada se zagrije, oslobađa zarobljene plinove i može se ponovno koristiti nekoliko puta.
-Zbog antimikrobnih svojstava srebra, njegov oksid je koristan u istraživanjima bioanalize i pročišćavanja tla.
-To je blago oksidirajuće sredstvo koje može oksidirati aldehide u karboksilne kiseline. Također se koristi u Hofmannovi reakciji (tercijarni amini) i sudjeluje u drugim organskim reakcijama, bilo kao reagens ili katalizator.
reference
- Bergstresser M. (2018). Srebrni oksid: Formula, razgradnja i formacija. Studija. Preuzeto s: study.com
- Autori i urednici svezaka III / 17E-17F-41C. (N. D.). Srebrni oksidi (Ag (x) O (y)) kristalna struktura, parametri rešetke. (Numerički podaci i funkcionalni odnosi u znanosti i tehnologiji), vol. 41C. Springer, Berlin, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Potencijalni utjecaj bioenergetskog tretmana na fizikalna i toplinska svojstva praha srebrnog oksida. Međunarodni časopis za biomedicinsku znanost i inženjerstvo. Svezak 3, br. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Raspadanje srebrnog oksida. Sveučilište Oregon Preuzeto s: chemdemos.uoregon.edu
- Flint, Deyanda. (24. travnja 2014.) Koristi od srebro-oksidnih baterija. Sciencing. Preuzeto s: sciencing.com
- Salman Montasir E. (2016). Proučavanje nekih optičkih svojstava srebrnog oksida (Ag2o) pomoću UVVisibilnog spektrofotometra. [PDF]. Preuzeto s: iosrjournals.org
- Bard Allen J. (1985). Standardni potencijali u vodenoj otopini. Marcel Dekker. Preuzeto s: books.google.co.ve


