Karakteristike proteinaze K, enzimska aktivnost i primjena
proteinaze K je enzim koji pripada grupi serinskih proteaza, to jest, ima u svom aktivnom katalitičkom središtu aminokiselinski serin i ima funkciju razbijanja peptidnih veza hidrolizom. Zauzvrat, ovaj enzim pripada obitelji proteina subtilizina (peptidaza S8).
Proteinaza K ima molekularnu težinu (MW) od 28.900 daltona i prvi put je izolirana 1974. godine iz ekstrakta gljivica Engyodontium album, ranije poznat pod imenom Tritirachium album Limber.
Predstavlja visoki proteolitički kapacitet, dokazano da može razgraditi keratin prisutan u kosi. Riječ keratin na engleskom jeziku je napisana "keratin", stoga je nazvana "proteinaza K".
Zbog svog visokog kapaciteta za cijepanje prirodnih proteina, ovaj enzim je koristan u raznim tehnikama molekularne biologije. Uglavnom se koristi za izolaciju i pripremu nukleinskih kiselina s visokom molekularnom težinom (MW).
Proteinaza K djeluje oslobađanjem nuklearne DNA, dok uništava proteine i inaktivira RNaze i DNaze, tj. Eliminira nukleaze u DNA i RNA pripravcima..
S druge strane, uočeno je da proteinaza K može hidrolizirati neke denaturirane prirodne proteine, što je pobudilo interes istraživača za njegovu upotrebu u proučavanju prionskih proteina (PrPC)..
Međutim, usprkos svojoj visokoj proteolitičkoj moći postoje proteini koji su otporni na djelovanje proteinaze K. Među njima, postoje neki abnormalni proteini koji se nazivaju prioni (PrPSc), povezani s transmisivnim spongiformnim encefalopatijama..
indeks
- 1 Značajke proteinaze K
- 2 Enzimatsko djelovanje
- 3 Aplikacije
- Prednosti proteinaze K
- Proteini otporni na proteinu K
- 6 Reference
Značajke proteinaze K
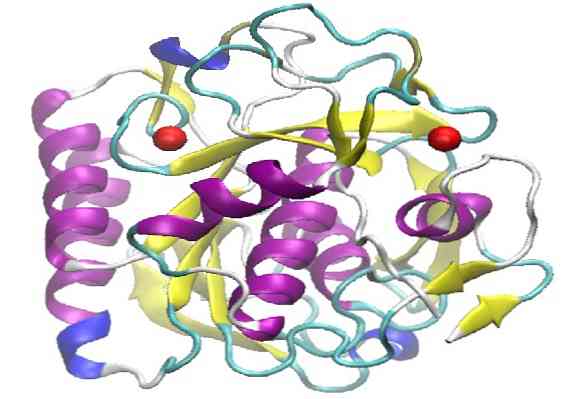
Proteinaza K ima tercijarnu strukturu formiranu s tri sloja, s ß-pločom od sedam lanaca raspoređenih između dva sloja spirale. Budući da pripada obitelji S8 peptidaza, karakterizira ga katalitička trijada u svom aktivnom mjestu, čiji je redoslijed redom (Asp, His i Ser), što ih razlikuje od drugih obitelji peptidaza..
Ovaj enzim iz skupine serinskih proteaza je karakteriziran hidrolizom peptidnih veza blizu karboksilne skupine alifatskih i aromatskih aminokiselina..
S druge strane, sposoban je djelovati u prisutnosti određenih korozivnih tvari, kao što su natrijev dodecil sulfat (SDS), Tris-HCL i EDTA, koje se koriste kao pomoć u denaturaciji proteina, uzrokujući gubitak izvorne strukture..
To je preliminarni korak u pripremi proteina za tehniku elektroforeze. Raspon pH kod kojeg djeluje proteinaza K je prilično širok (2,0 do 12,0), s optimalnim pH između 7,5 i 12,0, a njegova izoelektrična točka je 8,9. Kao što se može vidjeti, on je aktivan u vrlo širokom rasponu pH.
Još jedna značajka koja se ističe u proteinazi K je njegova stabilnost u prisustvu visokih temperatura (50 - 60 ° C).
Enzimska aktivnost
Proteinazi K potrebna je prisutnost kalcijevog iona, iako to ne utječe na njegovu aktivnost, ako je neophodno za održavanje njegove stabilnosti.
Da bi proteinaza K izvršila potpunu digestiju supstrata, potrebno je približno vrijeme kontakta između 5 minuta i 2 sata..
Međutim, u tom smislu Daza et al., Su uspoređivali čistoću DNA dobivene u nekoliko navrata izloženosti proteinazi K, i zaključili da produžena inkubacija (do 24 h) značajno poboljšava kvalitetu DNA.
Sada, u odnosu na koncentraciju enzima proteinaze K u različitim protokolima, može se reći da je vrlo raznolika.
Može se koristiti od vrlo niskih koncentracija (5 μg / ml) do koncentracija od 500 μg / ml. Najčešći radni rasponi kreću se u rasponu od 50-100 μg / ml, posebno za probavu proteina i inaktivaciju nukleaze. Iako je za liječenje tkiva potrebna koncentracija od 2 mg / ml.
aplikacije
Njegove su primjene vrlo široke i mogu se sažeti u sljedećem:
-Koristi se u probavi proteina i ekstrakciji DNA pomoću nekoliko metoda kao što su: isušivanje, PK-SDS, cetil-trimetil amonijev bromid (CTAB), modificirani kalijev acetat i ekstrakcija s natrijevim jodidom..
-Inaktivacija nukleaza (RNaze i DNaze).
-U hibridizacijskoj tehnici in situ (HIS), kako bi se olakšalo oslobađanje nukleinske kiseline, uz eliminiranje neželjenih proteina.
-Modifikacija proteina.
-Na razini istraživanja, u raznim studijama.
Prednosti proteinaze K
Provedeno je nekoliko komparativnih studija između tehnika ekstrakcije DNK korištenjem Proteinase K, s drugima koji ga ne koriste i svi zaključuju da postoje veće koristi kada se koristi enzim. Među prednostima može se spomenuti sljedeće:
-Dobivena je DNA visoke molekulske mase visoke kvalitete i čistoće.
-Ekstrahirana DNA je stabilna do 3 mjeseca.
Ekstrahirana DNA može se koristiti u sljedećim tehnikama: Southern blot, polimeraza lančana reakcija (PCR), elektroforeza, između ostalih.
Proteini rezistentni na proteinazu K
Različita istraživanja su zaključila da su prioni (abnormalni PrPSc toksični proteini) diferencirani od PrPC proteina (nativni) jer su otporni na djelovanje proteinaze K, dok su PrPC osjetljivi na njihovo djelovanje..
Drugi autori su opisali da u strukturi PrPSc postoje osjetljivi dijelovi i drugi otporni na proteinazu K. Međutim, oba su dijela jednako otrovna i infektivna..
S druge strane, Bastian i suradnici 1987. izdvojili su 4 proteina od 28, 30, 66 i 76 kda iz vrste Spiroplasma mirum. Svi su bili otporni na djelovanje proteinaze K i također su imali križnu reakciju s nekim prionima.
Poznato je da ova vrsta može uzrokovati katarakte i važna neurološka oštećenja, a zbog znanstvenih nalaza Bastiana, među ostalim istraživanjima, učinjen je pokušaj da se taj mikroorganizam poveže s transmisivnim spongiformnim encefalopatijama..
Međutim, etiologija ove degenerativne neurološke patologije još se danas pripisuje prionima.
U tom smislu, Butler i suradnici 1991. identificirali su i karakterizirali klasu proteina otpornog na proteinazu od 40 Kda iz dvaju sojeva Mycoplasma hyorhinis. Ovaj patogen utječe na svinje, zaraze njihova tkiva, ali u ovom slučaju nije bilo unakrsne reakcije s testiranim prionima.
Potrebno je više istraživanja kako bi se razjasnile mnoge nepoznanice o tome.
reference
- Bastian F, Jennings R, i Gardner W. 1987. Antiserum za fibrilnu bjelančevinu povezanu sa scrapie, unakrsno reagira s Spiroplasma mirum proteini fibrila. J. Clin. Microhiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Procjena metode ekstrakcije i pročišćavanja DNA iz mišićnog tkiva fiksiranog u formaldehidu od neidentificiranih leševa. Med Magazine, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E i Mcgarrity G. Identifikacija i karakterizacija proteina otpornih na proteazu K u pripadnicima klasnih molikula. Infection and Immunity, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et al. Usporedba dva protokola za izdvajanje DNA iz Trypanosoma cruzi uzgojen u aksenskom mediju. Rev. Peru. Med. Exp. Public Health 2014; 31 (2): 222-227. Dostupno na: scielo.org
- Jiménez G, Villalobos M, Jiménez E i Palma W. Određivanje učinkovitosti pet protokola za ekstrakciju DNA iz parafinskog materijala za molekularne studije. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


