Struktura, svojstva, sinteza, uporaba i rizici natrijevog benzoata
natrijev benzoat je organska sol čija je kemijska formula C6H5COONa. Dobiva se ili generira reakcijom neutralizacije između benzojeve kiseline i natrijevog hidroksida. Rezultat je bijela krutina (donja slika) topiva u vodi i razgrađuje se zagrijavanjem na 120 ° C.
Ova se sol može naći prirodno u raznim plodovima i drugim dijelovima povrća, kao što su: borovnice, šljive, grožđice, cimet, klinčići i jabuke. Također je metabolit algi i biljaka.

Natrijev benzoat se ne nakuplja u tijelu, jer se brzo kombinira s aminokiselinom glicinom u obliku hipurične kiseline, koja se slobodno izlučuje urinom..
Ovaj se spoj koristi s konzervansom hrane, a njegovo djelovanje je učinkovitije pri kiselom pH. To je zbog prisutnosti organskih kiselina koje daju hrani pH pogodan za djelovanje natrijevog benzoata; koja kao takva postaje protonirana u benzojevu kiselinu.
Ova se sol također koristi u liječenju nasljednih metaboličkih poremećaja ciklusa ureje, koji proizvodi akumulaciju intermedijernog metabolita, za koji je enzim koji ga obrađuje manjkav..
Međunarodni program o kemijskoj sigurnosti nije pronašao štetan učinak natrijeva benzoata na ljude, za potrošnju između 647 - 825 mg / kg tjelesne mase..
Međutim, prijavljeno je da natrijev benzoat može izazvati pseudo-alergijske reakcije i pogoršati simptome u bolesnika s čestim epizodama urtikarije i astme..
indeks
- 1 Struktura natrijeva benzoata
- 2 Svojstva
- 2.1 Kemijska imena
- 2.2 Fizički opis
- 2.3 Miris
- 2.4 Okus
- 2.5 Plamište
- 2.6 Automatsko paljenje
- 2.7 Gustoća
- 2.8 Topljivost
- 2.9 Stabilnost
- 2.10 Raspadanje
- 2,11 pH
- 2.12 Površinska napetost
- 3 Sažetak
- 4 Upotreba
- 4.1 U hrani
- 4.2 Liječenje
- 4.3 Ostalo
- 5 Rizici
- 6 Reference
Struktura natrijeva benzoata
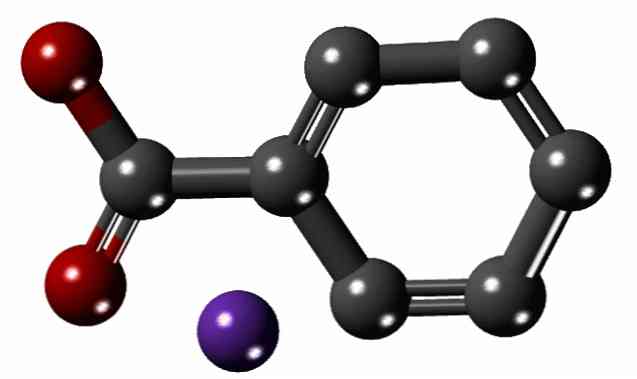
Na gornjoj slici prikazana je struktura natrijeva benzoata s modelom kuglica i šipki. Aromatski prsten se može vidjeti golim okom, s karboksilatnom skupinom, -COO-, s njom (crvenom); a potonji, pak, elektrostatički privlači Na kation+ (ljubičasta sfera).
Budući da je razlika u veličini između dvaju jona velika (usporedi na slici), nije iznenađujuće da je reticularna energija kristala natrijeva benzoata niska. To uzrokuje da njihovi kristali imaju prirodnu sklonost solubiliziranju u polarnim otapalima ili da trpe niz kemijskih reakcija.
C6H5COO- Može prihvatiti dva vodikova mosta iz dvije molekule vode, što pogoduje njegovoj hidrataciji. U međuvremenu, Na+ Također završava solvatiranom vodom, prevladavajući elektrostatske sile koje ga drže zajedno s C6H5COO-.
Dakle, ova sol se sastoji od C iona6H5COO- i Na+, koji su uređeni na uredan način za izgradnju kristala. U literaturi nisu dobivene informacije o njegovoj kristaliničnoj strukturi, tako da nije poznato kakav je tip jedinice za ovu sol.
nekretnine
Kemijska imena
-Natrijev benzoat
-Natrijeva sol benzojeve kiseline
-Sobenato
-Antimol.
Fizički opis
Bijele granule ili kristalni prah. Bezbojni kristalni prah.
miris
WC.
aroma
Gorko-slatko, trpko i neugodno.
Točka paljenja
> 100 ° C.
Automatsko paljenje
> 500 ° C.
gustoća
1,50 g / cm3.
topljivost
-Topiv u tekućem amoniju i piridinu.
-Blago topljiv u etanolu: 8,22 g / 100 g na 25 ºC.
-U metanolu je topiviji nego u etanolu: 8,22 g / 100 g na 15 ° C.
stabilnost
Stabilan je pod preporučenim uvjetima skladištenja. Može biti osjetljiv na vlagu i hidrolizirati u benzojevu kiselinu. Nekompatibilno s jakim oksidirajućim sredstvima, lužinama i mineralnim kiselinama.
raspad
Kada se zagrije na 120 ° C (248 ° F), ispušta jaki dim natrijevog oksida i drugih komponenti koje mogu biti otrovne i kancerogene.
Kada se razgradi na 120 ° C, sprječava se da se njegove točke vrenja i tališta mogu precizno odrediti, a navedene vrijednosti tih parametara su teoretske procjene..
pH
Blizu 8, otopljeno u vodi. To jest, to je bazična sol. To je zbog toga što hidrolizira kako bi oslobodila OH ione-.
Površinska napetost
72,9 mN / cm pri 20 ° C u otopini od 1 g / l vode.
sinteza
Benzojeva kiselina uključena u sintezu natrijevog benzoata proizvodi se uglavnom trima metodama:
-Naftalen se oksidira s vanadij pentoksidom da nastane ftalni anhidrid. Ovaj spoj može proći dekarboksilaciju da uzrokuje benzojevu kiselinu, budući da u svojoj strukturi s dva aromatska prstena čini se da imaju dvije -COO skupine kondenzirane zajedno.
-Toluen se oksidira u benzojevu kiselinu dodatkom dušične kiseline. U ovoj reakciji metil grupa "jednostavno" oksidira se u karboksilnu skupinu:
C6H5CH3 => C6H5COOH
-I konačno, benzotriklorid se hidrolizira djelovanjem mineralnih kiselina koje potječu iz benzojeve kiseline.
Dobivena benzojeva kiselina bilo kojom od ove tri metode, zatim je otopljena u natrijevom hidroksidu. Ovi spojevi prolaze reakciju neutralizacije, proizvodeći natrijev benzoat i vodu.
C6H5COOH + NaOH => C6H5COONa + H2O
Reakcija se također može provesti s natrijevim karbonatom, iako njegov prinos može biti manji od željenog.
aplikacije
U hrani
Natrijev benzoat je konzervans hrane, koji može inhibirati ili odgoditi proces fermentacije, zakiseljavanje ili bilo koji proces koji ih pogoršava. Osim toga, natrijev benzoat ima fungicidno djelovanje.
Ova sol može eliminirati kvasce, bakterije i gljivice prisutne u hrani. Njegovo konzervativno djelovanje je učinkovitije pri pH < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Natrijev benzoat se također koristi u očuvanju gaziranih pića i bezalkoholnih pića, u kojima je prisutna ugljična kiselina. Također u džemovima, bogatim limunskom kiselinom, i općenito u hrani s prisutnim kiselinama koje stvaraju kiselo okruženje.
Osim toga, koristi se u hrani s koncentracijom natrijevog benzoata od 0,1%. Maksimalna količina benzojeve kiseline i natrijeva benzoata, kao konzervansa u hrani, ne prelazi 2.000 mg / kg hrane.
Liječenje
Akutna hiperamonemija
Natrijev fenilacetat i natrijev benzoat koriste se u obliku adjuvantnih terapija u liječenju akutne hiperamonijemije i pridružene encefalopatije u bolesnika s promjenama ciklusa ureje.
Ovi spojevi su klasificirani kao lijekovi siročadi. Ovaj naziv vrijedi za lijekove koji nisu ekonomski isplativi.
shizofrenija
Natrijev benzoat se eksperimentalno koristi u liječenju shizofrenije. Središnji dio istraživanja je uloga koju u liječenju obavlja inhibicija enzima oksidaze D-amino kiselina, aktivnost koja zadovoljava natrijev benzoat.
Arginosukcinska kiselina
Natrijev benzoat se koristi u liječenju argininosukcinske acidurije, nasljednog metaboličkog poremećaja koji kod pacijenata može uzrokovati povećanje koncentracije amonijaka, koji može utjecati na središnji živčani sustav..
inhibicijska
-To je inhibitor enzima araquidonato 15-lipoksigenaze, enzima koji je istraživala farmaceutska industrija zbog uključenosti u koronarnu bolest srca.
-On inhibira djelovanje enzima lipaze triacilglicerida, enzima koji djeluje na oslobađanje glicerola i masnih kiselina u tankom crijevu, čime se omogućuje apsorpcija tih lipida prisutnih u hrani..
Može se koristiti natrijev benzoat za regulaciju crijevne apsorpcije lipida kao što su triacilgliceridi.
Nasljedni poremećaji
Natrijev benzoat se koristi u liječenju nekoliko nasljednih poremećaja povezanih s metabolizmom aminokiselina, među kojima se spominju: liječenje hiperergininemije i liječenje nedostatka enzima translokaze ornitina.
drugi
-Koristi se za ispiranje na bazi alkohola i za poliranje srebra. Osim toga, koristi se u izradi pirotehničkih spojeva, te je odgovoran za zviždaljku koja se proizvodi kada se zapali.
-Koristi se kao antikorozivna, što je jedan od glavnih zahtjeva u proizvodnji te soli. Također se koristi u rashladnim sredstvima, antifrizu i drugim sustavima na bazi vode.
-U formulaciji plastike kao što je polipropilen, ona se koristi za poboljšanje njegove čvrstoće i jasnoće.
-Služi kao stabilizator u kupaonicama i fotografskim procesima.
rizici
Natrijev benzoat je klasificiran od strane FDA kao "općenito siguran", u dozi od 0,1% težine hrane. Ne smatra se da iritira kontakt s kožom i očima, pa se može reći da je akutna toksičnost niska.
Međutim, natrijev benzoat može uzrokovati neimunološke reakcije (pseudoalergija) putem kontakta. Ovaj je učinak rijedak kod normalnih ljudi, ali u bolesnika s učestalim epizodama urtikarije ili simptoma astme može doći do povećanja učestalosti ovih simptoma..
U ispitivanjima na štakorima i miševima nisu nađeni dokazi o karcinogenom djelovanju natrijeva benzoata.
Istaknuta je neugodnost njezine uporabe u prisutnosti askorbinske kiseline, koja bi mogla proizvesti benzen; toksični spoj, označen kao kancerogen.
reference
- Neto industrije. (2019). Proizvodnja natrijevog benzoata. Preuzeto s: science.jrank.org
- Wikipedia. (2019). Natrijev benzoat. Preuzeto s: en.wikipedia.org
- Pubchem. (2019). Natrijev benzoat. Preuzeto s: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Činjenice o natrijevom benzoatu. Livestrong. Preuzeto s: livestrong.com
- Kemijska knjiga. (2017). Natrijev benzoat. Preuzeto s: chemicalbook.com
- Lane H. i sur. (2013) Jama Psichiatry. 70 (12): 1267-1275.
- Svjetska zdravstvena organizacija Ženeva. (12. travnja 2005.) Benzojeva kiselina i natrijev benzoat. [PDF]. Preuzeto s: who.int


