Model teorije traka i primjeri
teorije bendova je onaj koji definira elektroničku strukturu krutine kao cjeline. Može se primijeniti na bilo koju vrstu krutine, ali ona se nalazi u metalima gdje se odražavaju njegovi najveći uspjesi. Prema toj teoriji, metalna veza proizlazi iz elektrostatskog privlačenja između pozitivno nabijenih iona i pokretnih elektrona u kristalu..
Stoga metalni kristal ima "more elektrona", koji može objasniti njegova fizička svojstva. Donja slika prikazuje metalnu vezu. Ljubičaste točkice elektrona delokalizirane su u moru koje obuhvaća pozitivno nabijene atome metala.

"More elektrona" nastaje iz pojedinačnih doprinosa svakog atoma metala. Ovi doprinosi su njegove atomske orbitale. Metalne konstrukcije su općenito kompaktne; što su kompaktnije, to su veće interakcije između njihovih atoma.
Kao rezultat toga, njihove se atomske orbitale preklapaju da bi generirale vrlo uske molekularne orbitale u energiji. More elektrona je tada samo veliki skup molekularnih orbitala s različitim rasponima energija. Raspon tih energija čini ono što je poznato kao energetske trake.
Ove trake su prisutne u bilo kojem području kristala, zbog čega se smatra kao cjelina, a odatle dolazi definicija te teorije..
indeks
- 1 Model energetskih traka
- 1.1 Fermijeva razina
- 2 Poluvodiči
- 2.1. Intrinzični i vanjski poluvodiči
- 3 Primjeri primijenjene teorije bendova
- 4 Reference
Model energetskih traka

Kada s orbitalom metalnog atoma stupi u interakciju s onim susjeda (N = 2), formiraju se dvije molekularne orbitale: jedna veza (zeleni pojas) i jedna od anti-link (tamno crvena traka).
Ako je N = 3, sada se formiraju tri molekularne orbitale, od kojih je srednja (crna traka) neobvezujuća. Ako je N = 4, formiraju se četiri orbitale i razdvajaju one s najvećim obvezujućim karakterom i one s najvećim anti-zamrzivačkim karakterom..
Raspon raspoložive energije za molekularne orbitale se širi kako metalni atomi kristala daju svoje orbitale. To također rezultira smanjenjem energetskog prostora između orbitala, do točke da se kondenziraju u pojasu.
Ovaj pojas sastavljen od orbitala ima područja niske energije (zelene i žute boje) i visoke energije (one narančaste i crvene boje). Njihovi energetski ekstremi imaju nisku gustoću; međutim, većina molekularnih orbitala (bijela pruga) koncentrirana je u središtu.
To znači da elektroni "trče brže" kroz središte trake nego na svojim krajevima.
Razina Fermi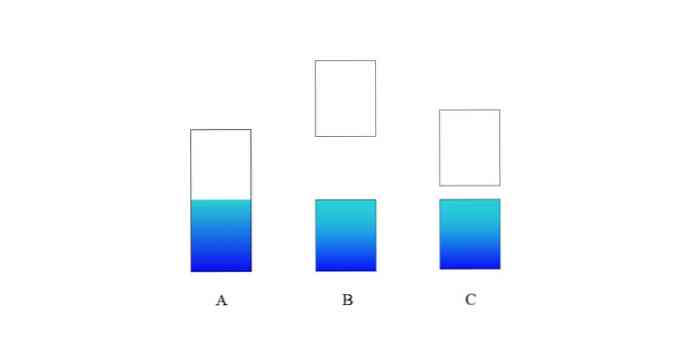
To je najveće energetsko stanje koje zauzimaju elektroni u krutini na apsolutnoj nultoj temperaturi (T = 0 K).
Jednom kada je pojas izgrađen, elektroni počinju zauzimati sve njihove molekularne orbitale. Ako metal ima jedan valentni elektron (e)1), svi elektroni u njenom kristalu zauzimat će polovicu trake.
Druga, nenastanjena polovica je poznata kao pokretna traka, dok je pojas pun elektrona nazvan valentni pojas.
U gornjoj slici A predstavlja tipičan valentni pojas (plavi) i provodni pojas (bijeli) za metal. Plava linija granice označava razinu Fermija.
Budući da metali također imaju p-orbitale, oni se kombiniraju na isti način da potječu p-pojas (bijeli).
U slučaju metala, s i p trake su vrlo bliske u energiji. To omogućuje njihovo preklapanje, potičući elektrone iz valentnog pojasa u provodni pojas. To se događa čak i na temperaturama malo iznad 0 K.
Za prijelazne metale i iz razdoblja 4 prema dolje, također je moguće formirati trake od.
Razina Fermija u odnosu na vodljivi pojas je vrlo važna za određivanje električnih svojstava.
Primjerice, metal Z s Fermijevom razinom vrlo blizu provodnog pojasa (najbližeg praznog pojasa u energiji) ima veću električnu vodljivost od X-metala u kojem je njegova Fermijeva razina daleko od te trake..
Poluvodiči
Električna vodljivost tada se sastoji od migracije elektrona iz valentnog pojasa u provodni pojas.
Ako je energetski razmak između obje trake vrlo velik, imamo izolacijsku krutinu (kao kod B). S druge strane, ako je ta praznina relativno mala, čvrsta tvar je poluvodič (u slučaju C).
Suočeni s porastom temperature, elektroni u valentnoj zoni dobivaju dovoljno energije da migriraju prema provodnom pojasu. To rezultira električnom strujom.
Zapravo, radi se o kvaliteti krutih ili poluvodičkih materijala: na sobnoj temperaturi su izolatori, ali na visokim temperaturama oni su vodiči.
Unutarnji i vanjski poluvodiči

Unutarnji vodiči su oni u kojima je energetski razmak između valentnog pojasa i provodnog pojasa dovoljno mali da toplinska energija dopušta prolaz elektrona.
S druge strane, vanjski vodiči pokazuju promjene u svojim elektroničkim strukturama nakon dopiranja nečistoćama, koje povećavaju njihovu električnu vodljivost. Ta nečistoća može biti drugi metal ili nemetalni element.
Ako nečistoća ima više valentnih elektrona, može osigurati donorsku traku koja služi kao most za prijelaz elektrona valentne trake u provodni pojas. Te su krute tvari n-tip poluvodiča. Ovdje n oznaka dolazi iz "negativnog".
U gornjoj slici donorska traka je prikazana u plavom bloku odmah ispod trake za vožnju (Tip n).
S druge strane, ako nečistoća ima manje valentnih elektrona, ona osigurava akceptorski pojas, koji skraćuje energetski razmak između valentnog pojasa i trake..
Elektroni prvo migriraju prema tom pojasu, ostavljajući iza sebe "pozitivne rupe", koje se kreću u suprotnom smjeru.
Kako ovi pozitivni razmaci označavaju prolaz elektrona, krutina ili materijal je poluvodič p-tipa..
Primjeri primijenjene teorije bendova
- Objasnite zašto su metali svijetli: njihovi pokretni elektroni mogu apsorbirati zračenje u širokom rasponu valnih duljina kada skoče na više razine energije. Zatim emitiraju svjetlost, vraćajući se na niže razine pogonskog pojasa.
- Kristalni silicij je najvažniji poluvodički materijal. Ako je dio silikona dopiran tragovima elementa grupe 13 (B, Al, Ga, In, Tl), on postaje poluvodič p-tipa. Ako je dopiran elementom skupine 15 (N, P, As, Sb, Bi), on postaje poluvodič n-tipa.
- Svjetleća dioda (LED) je spojeni poluvodič p-n. Kako to misliš? Da materijal ima oba tipa poluvodiča, i n i p. Elektroni migriraju iz provodnog područja poluvodiča n-tipa, u valentni pojas poluvodiča p-tipa.
reference
- Whitten, Davis, Peck & Stanley. Kemija. (8. izdanje). CENGAGE Learning, str. 486-490.
- Shiver & Atkins. (2008). Anorganska kemija (Fourth edition., Str. 103-107, 633-635). Mc Graw Hill.
- Brod C.R. (2016). Band teorija čvrstih tvari. Preuzeto 28. travnja 2018., iz: hyperphysics.phy-astr.gsu.edu
- Steve Kornić (2011). Prelazak s obveznica na bendove s kemijske točke gledišta. Preuzeto 28. travnja 2018. iz: chembio.uoguelph.ca
- Wikipedia. (2018.). Vanjski poluvodič. Preuzeto 28. travnja 2018. s adrese: en.wikipedia.org
- Byju'S. (2018.). Band-teorija metala. Preuzeto 28. travnja 2018. od: byjus.com



